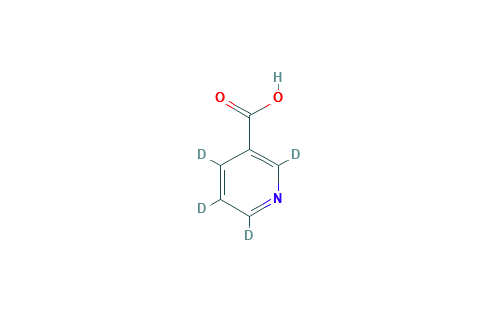
Τι είναι η βιταμίνη Β3, ή αλλιώς νιασίνη και ποιά η δράση της;
Η νιασίνη (βιταμίνη Β3) είναι μια υδατοδιαλυτή βιταμίνη του συμπλέγματος των βιταμινών Β. Νιασίνη είναι ο γενικός όρος, ο οποίος χρησιμοποιείται για να περιγράψει τα συστατικά που παρουσιάζουν τις βιολογικές ιδιότητες του νικοτιναμιδίου. Στην τροφή συναντάται ως νικοτιναμίδιο και νικοτινικό οξύ.
Είναι γνωστή και ως νιασιναμίδιο. Γνωστή και ως βιταμίνη Β3 το όνομα «νιασίνη» επιλέχθηκε, προκειμένου να αποφευχθεί η συνειρμική διασύνδεση της βιταμίνης με το κάπνισμα, που οφειλόταν στη χρήση του όρου «νικοτινικό οξύ».
Δράση
Ως βιταμίνη, η νιασίνη λειτουργεί σαν συστατικό 2 συνενζύμων. Τα συγκεκριμένα συνένζυμα συμμετέχουν σε πολλές μεταβολικές διεργασίες, όπως στη γλυκόλυση, στην κυτταρική αναπνοή και στο μεταβολισμό των λιπών, των πουρινών και των αμινοξέων.
Αποτελεί δομικό συστατικό του νικοτιναμιδο-αδενινο-δινουκλεοτιδίου (NAD+/NADH), που αποτελεί συνένζυμο στις οξειδοαναγωγικές αντιδράσεις της αναπνευστικής αλυσίδας των μιτοχονδρίων (οξειδωτική φωσφορυλίωση). Αποτελεί, επίσης, δομικό συστατικό του φωσφορικού νικοτιναμιδο-αδενινο-δινουκλεοτιδίου (NADP/NADPH2), όπου παίζει σημαντικό ρόλο, ως συνένζυμο μεταφοράς υδρογόνου.
Χρήση
Παρόλο που έχουν διατυπωθεί ισχυρισμοί για τη χρήση της νιασίνης στην αρθρίτιδα, στη σχιζοφρένια και σε άλλες ψυχικές διαταραχές, στην εξάρτηση από το αλκοόλ, αυτές δεν έχουν ακόμα αποδειχθεί. Το νικοτινικό οξύ μπορεί να χορηγηθεί με ιατρική συνταγή για την υπερλιπιδαιμία.
Το νικοτινικό οξύ έχει χρησιμοποιηθεί και ως φάρμακο για την αντιμετώπιση της υπερχοληστερολαιμίας, σε δόσεις μεγαλύτερες της συνιστώμενης ημερήσιας πρόσληψης. Στις δόσεις αυτές μπορεί να προκαλέσει αγγειοδιαστολή, με αποτέλεσμα την εμφάνιση υπότασης, ερυθρότητας και εξάψεων.
Υπερδοσολογία
Σε δόσεις πάνω από τις διατροφικές απαιτήσεις, το νικοτινικό οξύ (όχι όμως και το νικοτιναμίδιο) μειώνει τη χοληστερόλη ορού και τα τριγλυκερίδια, παρεμποδίζοντας τη σύνθεση των πολύ χαμηλής περιεκτικότητας λιποπρωτεινών (VLDL), οι οποίες είναι πρόδρομοι των χαμηλής περιεκτικότητας λιποπρωτεινών (LDL). Το νικοτινικό οξύ προκαλεί επίσης άμεση περιφερική αγγειοδιαστολή.
Είναι προτιμότερο να αποφεύγονται μεγάλες δόσεις νιασίνης σε περιπτώσεις ουρικής αρθρίτιδας (μπορεί να αυξήσει τα επίπεδα ουρικού οξέος), στο πεπτικό έλκος (μπορεί να ενεργοποιήσει ένα έλκος) και στις ηπατικές παθήσεις (πιθανή επιδείνωση). Οι μεγάλες δόσεις θα πρέπει επίσης να χρησιμοποιούνται με προσοχή στο σακχαρώδη διαβήτη. Τα συμπληρώματα με νικοτινικό οξύ δεν θα πρέπει να χρησιμοποιούνται για τη μείωση των επιπέδων χοληστερόλης χωρίς ιατρική έγκριση.
Ωστόσο υπάρχουν τιμές ανεκτικότητας ενός οργανισμού σε νιασίνη και παρατίθενται στον πίνακα
| ΑΝΩΤΕΡΕΣ ΦΥΙΟΛΟΓΙΚΕΣ ΤΙΜΕΣ ΠΡΟΣΛΗΨΗΣ ΝΙΑΣΙΝΗΣ | |
| Επίπεδο Ηλικίας | (mg/day) |
| Νήπια 0-12 μηνών | Δεν είναι γνωστή η ποσότητα * |
| Παιδιά 1-3 χρόνων | 10 |
| Παιδιά 4-8 χρόνων | 15 |
| Παιδιά 9-13 χρόνων | 20 |
| Έφηβοι 14-18 χρόνων | 30 |
| Ενήλικες 19 χρόνων + | 35 |
Ανεπιθύμητες ενέργειες
Το νικοτινικό οξύ και το νικοτιναμίδιο μπορεί να είναι τοξικά σε μεγάλες ποσότητες, αλλά οι ανεπιθύμητες ενέργειές τους διαφέρουν.
Νικοτιναμίδιο
Σε φυσιολογικές δόσεις, το νικοτιναμίδιο δεν είναι τοξικό, αλλά η χρόνια χορήγηση σε δόσεις 3 g ημερησίως για περιόδους μεγαλύτερες από 3 μήνες μπορεί να προκαλέσει ναυτία, πονοκεφάλους, καυσαλγία, κούραση, πονόλαιμο, ξηρά μαλλιά και δέρμα, θαμπή όψη.
Νικοτινικό οξύ
Σε δόσεις 100-200 mg παρατηρούνται συμπτώματα όπως οξεία έξαψη, πονοκέφαλοι, ζαλάδες, ναυτία, κνησμός, έμετοι, περιστασιακά περιορισμένη αντοχή στη γλυκόζη, αυξημένα επίπεδα ουρικού οξέος, σπάνια ηπατική βλάβη (συχνότερα όταν χορηγούνται σκευάσματα βραδείας αποδέσμευσης) και υπέρταση.
Αλληλεπιδράσεις
Φάρμακα/ Θρεπτικά συστατικά
Σε συνδυασμό με φάρμακα για τη μείωση των λιπιδίων μπορεί να υπάρξει κίνδυνος για ραβδομυόλυση (προκαλείται από μυική βλάβη και μπορεί να οδηγήσει σε οξεία νεφρική ανεπάρκεια) και μυοπάθεια. Η συνδυασμένη θεραπεία απαιτεί προσεκτική παρακολούθηση.
Ανεπάρκεια
Η έλλειψη της νιασίνης προκαλεί τη νόσο πελλάγρα. Η ανεπάρκεια, ή η περίσσεια μίας εκ των βιταμινών Β προκαλεί διαταραχές στο μεταβολισμό των άλλων. Έρευνες δείχνουν ότι ο ιός HIV αυξάνει τον κίνδυνο ανεπάρκειας της νιασίνης.
Συμπτώματα
Η πελλάγρα χαρακτηρίζεται από νευρολογικά συμπτώματα (ψευδαισθήσεις και παραλήρημα), διάρροια, βλεννογονίτιδα και δερματικές βλάβες με φαιά χροιά, που παρατηρούνται στις περιοχές του δέρματος που εκτίθενται στο φως.
Συνιστώμενη πρόσληψη
Ο πίνακας που ακολουθεί περιλαμβάνει τη συνιστώμενη πρόσληψη της νιασίνης σε mg ημερησίως στα διάφορα επίπεδα ηλικίας.
| ΣΥΝΙΣΤΩΜΕΝΗ ΠΡΟΣΛΗΨΗ ΓΙΑ ΝΙΑΣΙΝΗ | |||
| Επίπεδο Ηλικίας | Ηλικία | Άρρεν (mg NE*/day) | Θήλυ (mg NE/day) |
| Βρέφη | 0-6 months | 2 (AI) | 2 (AI) |
| Βρέφη | 7-12 months | 4 (AI) | 4 (AI) |
| Παιδιά | 1-3 years | 6 | 6 |
| Παιδιά | 4-8 years | 8 | 8 |
| Παιδιά | 9-13 years | 12 | 12 |
| Έφηβοι | 14-18 years | 16 | 14 |
| Ενήλικες | 19 years and older | 16 | 14 |
| Εγκυμοσύνη | all ages | – | 18 |
| Θηλασμός | all ages | – | 17 |
*NE, niacin equivalent: 1 mg NE(Ισοδύναμο Νιασίνης = 60 mg τρυπτοφάνης= 1 mg νιασίνης
Ηλικιωμένοι(65 χρόνων+) : Έρευνες δείχνουν ότι τά άτομα άνω των 65 χρόνων δεν προσλαμβάνουν ικανοποιητική ποσότητα νιασίνης που να φτάνει τη συνιστώμενη ημερήσια δόση. (16mg ΝΕ για άνδρες και 14mg ΝΕ για γυναίκες). Ωστόσο με τη χορήγηση ενός συμπληρώματος που περιέχει νιασίνη, τους παρέχονται τουλάχιστον 20mg νιασίνης ημερησίως.
Τροφές πλούσιες σε Νιασίνη
| Τρόφιμο | Ποσότητα | Νιασίνη (mg) |
| Κοτόπουλο | 90 γραμμάρια μαγειρεμένο χωρις πέτσα | 7.3 |
| Γαλοπούλα | 90 γραμμάρια μαγειρεμένο χωρις πέτσα | 5.8 |
| Βοδινό | 90 γραμμάρια μαγειρεμένο | 3.1 |
| Σολωμός | 90 γραμμάρια μαγειρεμένος | 8.5 |
| Τόνος(σε νερό) | 90 γραμμάρια | 11.3 |
| Ψωμί πολύσπορο | 1 φέτα | 1.3 |
| Δημητριακά πρωινού | 1 φλιτζάνι | 5-7 |
| Δημητριακά πρωινού εμπλουτισμένα | 1 φλιτζάνι | 20-27 |
| Ζυμαρικά | 1 φλιτζάνι (μαγειρεμένα) | 2.3 |
| Φυστίκια | 30γρ (ψημένα) | 3.8 |
| Φακές | 1 φλιτζάνι (μαγειρεμένες) | 2.1 |
| Γίγαντες | 1 φλιτζάνι (μαγειρεμένοι) | 1.8 |
| Καφές | 1 φλιτζάνι | 0.5 |
Βιβλιογραφία
- Linus Pauling Institute
- Brody T. Nutritional Biochemistry. 2nd ed. San Diego: Academic Press; 1999.
- Cervantes-Laurean D, McElvaney NG, Moss J. Niacin. In: Shils M, Olson JA, Shike M, Ross AC, eds. Modern Nutrition in Health and Disease. 9th ed. Baltimore: Williams & Wilkins; 1999:401-411.
- Jacob R, Swenseid M. Niacin. In: Ziegler EE, Filer LJ, eds. Present Knowledge in Nutrition. 7th ed. Washington D.C: ILSI Press; 1996:185-190.
- Jacobson MK, Jacobson EL. Discovering new ADP-ribose polymer cycles: protecting the genome and more. Trends Biochem Sci. 1999;24(11):415-417.
- Park YK, Sempos CT, Barton CN, Vanderveen JE, Yetley EA. Effectiveness of food fortification in the United States: the case of pellagra. Am J Public Health. 2000;90(5):727-738.
- Gregory JF, 3rd. Nutritional Properties and significance of vitamin glycosides. Annu Rev Nutr. 1998;18:277-296.
- Fu CS, Swendseid ME, Jacob RA, McKee RW. Biochemical markers for assessment of niacin status in young men: levels of erythrocyte niacin coenzymes and plasma tryptophan. J Nutr. 1989;119(12):1949-1955.
- Food and Nutrition Board, Institute of Medicine. Niacin. Dietary Reference Intakes: Thiamin, Riboflavin, Niacin, Vitamin B6, Vitamin B12, Pantothenic Acid, Biotin, and Choline. Washington, D.C.: National Academy Press; 1998:123-149.
- Jacobson EL, Jacobson MK. Tissue NAD as a biochemical measure of niacin status in humans. Methods Enzymol. 1997;280:221-230.
- Jacobson EL, Shieh WM, Huang AC. Mapping the role of NAD metabolism in prevention and treatment of carcinogenesis. Mol Cell Biochem. 1999;193(1-2):69-74.
- Hageman GJ, Stierum RH. Niacin, poly(ADP-ribose) polymerase-1 and genomic stability. Mutat Res. 2001;475(1-2):45-56.
- Boyonoski AC, Spronck JC, Gallacher LM, et al. Niacin deficiency decreases bone marrow poly(ADP-ribose) and the latency of ethylnitrosourea-induced carcinogenesis in rats. J Nutr. 2002;132(1):108-114.
- Gensler HL, Williams T, Huang AC, Jacobson EL. Oral niacin prevents photocarcinogenesis and photoimmunosuppression in mice. Nutr Cancer. 1999;34(1):36-41.
- Weitberg AB. Effect of nicotinic acid supplementation in vivo on oxygen radical-induced genetic damage in human lymphocytes. Mutat Res. 1989;216(4):197-201.
- Hageman GJ, Stierum RH, van Herwijnen MH, van der Veer MS, Kleinjans JC. Nicotinic acid supplementation: effects on niacin status, cytogenetic damage, and poly(ADP-ribosylation) in lymphocytes of smokers. Nutr Cancer. 1998;32(2):113-120.
- Jacobson EL. Niacin deficiency and cancer in women. J Am Coll Nutr. 1993;12(4):412-416.
- Negri E, Franceschi S, Bosetti C, et al. Selected micronutrients and oral and pharyngeal cancer. Int J Cancer. 2000;86(1):122-127.
- Franceschi S, Bidoli E, Negri E, et al. Role of macronutrients, vitamins and minerals in the aetiology of squamous-cell carcinoma of the oesophagus. Int J Cancer. 2000;86(5):626-631.
- Lampeter EF, Klinghammer A, Scherbaum WA, et al. The Deutsche Nicotinamide Intervention Study: an attempt to prevent type 1 diabetes. DENIS Group. Diabetes. 1998;47(6):980-984.
- Greenbaum CJ, Kahn SE, Palmer JP. Nicotinamide’s effects on glucose metabolism in subjects at risk for IDDM. Diabetes. 1996;45(11):1631-1634.
- Schatz DA, Bingley PJ. Update on major trials for the prevention of type 1 diabetes mellitus: the American Diabetes Prevention Trial (DPT-1) and the European Nicotinamide Diabetes Intervention Trial (ENDIT). J Pediatr Endocrinol Metab. 2001;14 Suppl 1:619-622.
- Knopp RH. Drug treatment of lipid disorders. N Engl J Med. 1999;341(7):498-511.
- Canner PL, Berge KG, Wenger NK, et al. Fifteen year mortality in Coronary Drug Project patients: long-term benefit with niacin. J Am Coll Cardiol. 1986;8(6):1245-1255.
- Guyton JR, Capuzzi DM. Treatment of hyperlipidemia with combined niacin-statin regimens. Am J Cardiol. 1998;82(12A):82U-84U; discussion 85-86U.
- Brown BG, Zhao XQ, Chait A, et al. Simvastatin and niacin, antioxidant vitamins, or the combination for the prevention of coronary disease. N Engl J Med. 2001;345(22):1583-1592.
- Cheung MC, Zhao XQ, Chait A, Albers JJ, Brown BG. Antioxidant supplements block the response of HDL to simvastatin-niacin therapy in patients with coronary artery disease and low HDL. Arterioscler Thromb Vasc Biol. 2001;21(8):1320-1326.
- McKenney J. New perspectives on the use of niacin in the treatment of lipid disorders. Arch Intern Med. 2004;164(7):697-705.
- Wink J, Giacoppe G, King J. Effect of very-low-dose niacin on high-density lipoprotein in patients undergoing long-term statin therapy. Am Heart J. 2002;143(3):514-518.
- Kashyap ML, McGovern ME, Berra K, et al. Long-term safety and efficacy of a once-daily niacin/lovastatin formulation for patients with dyslipidemia. Am J Cardiol. 2002;89(6):672-678.
- Brown RR, Ozaki Y, Datta SP, Borden EC, Sondel PM, Malone DG. Implications of interferon-induced tryptophan catabolism in cancer, auto-immune diseases and AIDS. Adv Exp Med Biol. 1991;294:425-435.
- Murray MF, Langan M, MacGregor RR. Increased plasma tryptophan in HIV-infected patients treated with pharmacologic doses of nicotinamide. Nutrition. 2001;17(7-8):654-656.
- Tang AM, Graham NM, Saah AJ. Effects of micronutrient intake on survival in human immunodeficiency virus type 1 infection. Am J Epidemiol. 1996;143(12):1244-1256.
- Hendler SS, Rorvik DR, eds. PDR for Nutritional Supplements. Montvale: Medical Economics Company, Inc; 2001
- Drug Facts and Comparisons. St. Louis: Facts and Comparisons; 2000:6-33.
- Knopp RH. Evaluating niacin in its various forms. Am J Cardiol. 2000;86(12A):51L-56L.
- Brown BG, Cheung MC, Lee AC, Zhao XQ, Chait A. Antioxidant vitamins and lipid therapy: end of a long romance? Arterioscler Thromb Vasc Biol. 2002;22(10):1535-1546.
- Flodin N. Pharmacology of micronutrients. New York: Alan R. Liss, Inc.; 1988.